發布日期:2024 - 06 - 26

醫藥工業百強

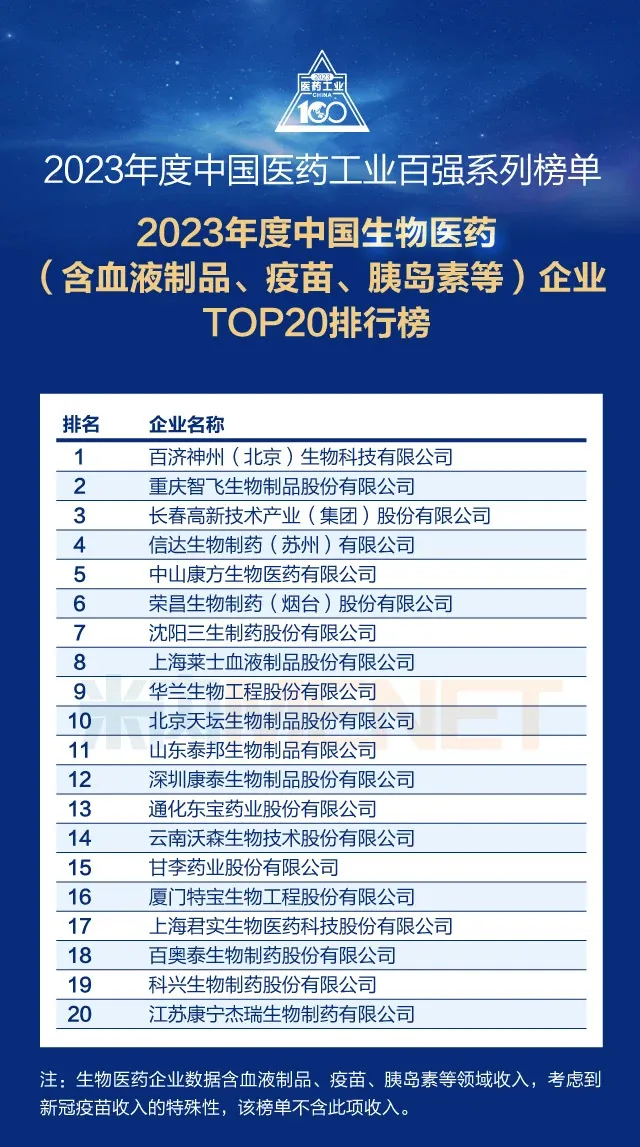
6月25日,在2024米思會上,針對醫藥工業企業從兩大重要維度——“創新驅動力”和“專業推廣力”出發評定的“2023年度中國醫藥工業百強系列榜單”評選結果重磅發布。科興制藥(688136.SH)連續第三年憑借扎實的研發創新力和亮眼的市場推廣能力,榮登“2023年度中國醫藥工業百強系列榜單”子榜單“中國生物醫藥(含血液制品、疫苗、胰島素等)企業TOP20排行榜”!

本次評選聚焦醫藥工業企業創新驅動力和專業推廣力,創新驅動力主要從企業研發投入R&D綜合指標進行評判,專業推廣力則重點根據臨床醫生和患者的最終選擇需求所決定的終端定量數據來剛性定義,最終結合米內網獨家的三大終端六大市場終端數據(定義范圍見下圖)進行定量分析。

入選企業的總分由兩部分構成,一是企業的創新驅動力,即2023年研發投入R&D綜合指標得分,占40%權重;二是企業的專業推廣力,即2023年臨床醫生和患者的最終選擇需求所決定的終端定量數據來剛性定義,也就是結合米內網獨家的三大終端六大市場終端數據進行定量分析的得分,占60%權重。
在創新驅動力方面,作為科創板上市公司,科興制藥始終堅定以研發創新驅動企業發展。根據2023年年報,近年來,公司圍繞重點聚焦的疾病領域,已立項創新藥項目10個,完成了多個新藥PCC分子創制,其中多個項目進入工藝開發階段,獲得了高純度、低成本、穩健可靠的生產工藝,并陸續開展非臨床研究。通過多個抗體創新藥的分子創制,驗證了雙抗和多抗分子設計的技術路徑,申請了多個專利,形成了公司抗體藥物設計的特色技術。
同時,公司不斷推進在研項目進度,并獲得實質進展,多個項目正競速臨床階段。包括人干擾素α1b吸入溶液Ⅲ期臨床受試者已入組,聚乙二醇化人粒細胞刺激因子注射液完成Ⅰ期臨床,人生長激素注射液進入Ⅰ期臨床、GB08注射液(FC長效生長激素)Ⅰ期臨床首例受試者入組已完成。其中,聚乙二醇化人粒細胞刺激因子注射液是一款升白藥,作為抗腫瘤一線用藥,在全球抗腫瘤治療中發揮重大作用,特別是在拉美、東南亞等新興市場國家存在較大的未滿足的臨床需求,根據DataBridgeMarketResearch數據顯示,預計2030年全球升白藥市場規模約60億美金,并且該管線可與公司原有短效GC產品形成合力,協同發展。
另一款重磅研發項目——人干擾素α1b吸入溶液,成功上市后有望成為國內首批治療兒童RSV感染的對癥藥物。根據《柳葉刀》發表的全球兒童RSV疾病負擔研究顯示,2019年全球5歲以下兒童中發生了3300萬例由RSV感染引起的急性下呼吸道感染,我國2019年5歲以下兒童RSV急性下呼吸道感染發病共約350萬例,占全球10%以上。
作為公司創新研發的堅實后盾,公司產品在市場推廣和市占率上一直保持強勁勢頭。2023年,公司核心產品終端覆蓋各等級醫院、基層醫療機構、藥店等約22,700家,較上年末增加約2,700家,其中醫院超7,500家,第三終端超10,700家,藥店約4,500家。
根據北京國藥誠信的數據結果顯示,2023年公司“賽若金®”國內短效注射用人干擾素的市場占有率保持排名第一;“依普定®”在國內人促紅素的市場占有率排名第二,市場占有率進一步提升;“白特喜®”在短效人粒細胞刺激因子市場排名由第七躍升至第五。
“出海”是中國醫藥產業發展壯大的必然趨勢,作為一家以高品質生物藥領導者為長期愿景的企業,科興制藥早已圍繞“創新+國際化”提前布局海外商業化。
自上市以來,科興制藥積極開展產品引進,不斷擴充產品線,累計引進了13款產品,同四十余個國家與客戶簽約并陸續提交了引進產品的注冊申請。其中,首個引進產品白蛋白紫杉醇也已獲得歐盟GMP的認證,使得公司國際化戰略邁上新的臺階。而其他如英夫利西單抗、貝伐珠單抗、阿達木單抗等多款產品有的也已相繼完成埃及、巴西、印尼等國的現場審計,預計將在2024年實現海外銷售。多個品種出海進程加速,不僅是科興制藥海外市場先發優勢的體現,更有望為公司業績的表現帶來積極影響,科興制藥長期以來對海外市場的深度耕耘,或即將迎來豐收期。

本次獲得中國醫藥工業百強系列排行榜的肯定,彰顯了科興制藥在國內醫藥工業領域的專業力和品牌影響力。未來,公司也將通過創新和迭代應對市場的不確定性,進化韌性力量,堅持高質量發展,把握新時代生物經濟機遇,繼續通過扎實的創新驅動力、專業推廣力和高質量的企業經營管理能力,攻堅制勝,繼續秉承“精益制藥,精益用藥,守護健康”的使命,用生物技術服務患者,成為高品質生物藥領導者!